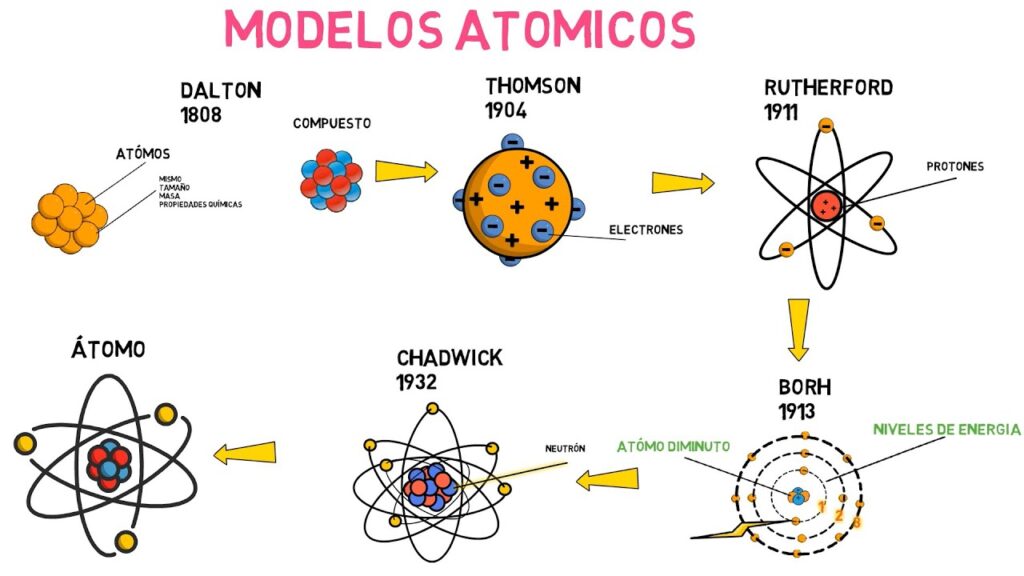
A evolução dos modelos atômicos foi essencial para a compreensão da estrutura da matéria. Diversos cientistas contribuíram para o avanço dessa teoria,
e seus modelos foram se aperfeiçoando ao longo do tempo. Vamos explorar os modelos propostos por Dalton, Thomson, Rutherford e Bohr.
O primeiro modelo moderno do átomo foi proposto por John Dalton, conhecido como “Modelo da Bola de Bilhar”. Dalton acreditava que os átomos eram
pequenas partículas esféricas e indivisíveis, como bolinhas sólidas. Suas principais ideias foram:
1. Átomo indivisível: Dalton sugeriu que os átomos não podiam ser divididos ou destruídos.
2. Átomos idênticos: Átomos de um mesmo elemento têm a mesma massa e propriedades, enquanto átomos de elementos diferentes possuem massas e propriedades distintas.
3. Reações químicas: Para Dalton, reações químicas eram apenas rearranjos de átomos.
Exemplos:
– O carbono e o oxigênio, ao se combinarem, formam o dióxido de carbono (CO2). Nesse processo, os átomos de carbono e oxigênio não são alterados, apenas rearranjados.
– Um cubo de ferro é formado por bilhões de átomos de ferro, todos idênticos entre si.
– A água é formada por átomos de hidrogênio e oxigênio, que se combinam em proporções específicas (H2O).
Joseph John Thomson descobriu o elétron e propôs o “Modelo do Pudim de Passas”. Segundo esse modelo, o átomo seria uma esfera de carga positiva, com elétrons
negativos espalhados pela superfície, como passas em um pudim. As ideias principais são:
1. Átomo divisível: Thomson foi o primeiro a sugerir que o átomo não era indivisível, como Dalton acreditava, mas composto de partículas subatômicas.
2. Esfera positiva: O átomo seria uma esfera de carga positiva, e os elétrons, de carga negativa, estariam distribuídos dentro dessa esfera.
3. Átomo neutro: A carga total do átomo seria neutra, já que a carga positiva da esfera equilibrava as cargas negativas dos elétrons.
Exemplos:
– Se você imaginar um átomo de sódio (Na) como uma esfera positiva com pequenos pontos negativos (elétrons) dispersos, você teria uma visão do “pudim de passas”.
– Um pedaço de pão com uvas passas poderia ser uma analogia: o pão representa a carga positiva e as passas, os elétrons.
– Em um átomo de carbono, os elétrons estariam distribuídos pela esfera de carga positiva.
Ernest Rutherford, após o experimento da “folha de ouro”, propôs o “Modelo Nuclear”. Ele demonstrou que o átomo tinha um núcleo pequeno e denso, com
carga positiva, rodeado por elétrons em órbita. Os principais pontos do modelo são:
1. Núcleo central: A maior parte da massa do átomo está concentrada em um núcleo pequeno e denso, composto de prótons.
2. Elétrons em órbita: Os elétrons orbitam o núcleo, assim como os planetas orbitam o Sol.
3. Átomo vazio: Rutherford concluiu que a maior parte do átomo é composta de espaço vazio.
Exemplos:
– Um átomo de hidrogênio teria um núcleo (próton) no centro e um elétron orbitando ao redor.
– Em um átomo de oxigênio, o núcleo conteria prótons e nêutrons, e os elétrons estariam em órbita ao redor dele.
– Imagine o núcleo de um átomo como uma bola de tênis e os elétrons orbitando a metros de distância.
Niels Bohr aperfeiçoou o modelo de Rutherford ao sugerir que os elétrons ocupam órbitas específicas, ou camadas de energia. Sua teoria é conhecida como “Modelo Quantizado de Bohr”.
Os principais pontos são:
1. Órbitas estacionárias: Os elétrons giram em órbitas fixas ao redor do núcleo, sem perder energia.
2. Níveis de energia: Cada órbita tem um nível de energia específico. Os elétrons podem saltar entre essas órbitas quando absorvem ou liberam energia.
3. Espectro de emissão: A luz emitida por um átomo, como o hidrogênio, é causada por elétrons saltando entre diferentes níveis de energia.
Exemplos:
– Quando um elétron de um átomo de hidrogênio absorve energia, ele pode saltar para uma órbita de energia mais alta.
– Se um átomo de sódio emite luz, isso significa que um elétron saltou de uma órbita de energia mais alta para uma mais baixa, liberando energia.
– O espectro de luz emitido por estrelas pode ser explicado pelo modelo de Bohr, com elétrons saltando entre níveis de energia.